Um estudo conduzido por pesquisadores da Universidade Harvard, nos Estados Unidos, concluiu que a esclerose múltipla — doença degenerativa para a qual não há cura — provavelmente está associada a uma infecção prévia pelo VEB (vírus Epstein-Barr).
Os resultados foram publicados no último dia 13 na renomada revista Science. "Este é o primeiro estudo que fornece evidências convincentes de causalidade", disse em comunicado o professor de epidemiologia e nutrição Alberto Ascherio, da Escola de Saúde Pública T.H. Chan, da Universidade Harvard.
A esclerose múltipla é uma doença autoimune que ataca o sistema nervoso central levando à incapacidade total do indivíduo em casos mais severos.
Os sintomas incluem formigamento nas extremidades, no tronco ou na face, fraqueza ou atitudes desajeitadas em um membro inferior ou na mão e distúrbios visuais. A doença afeta também a parte cognitiva, levando a quadros de desatenção e dificuldade de julgamento.
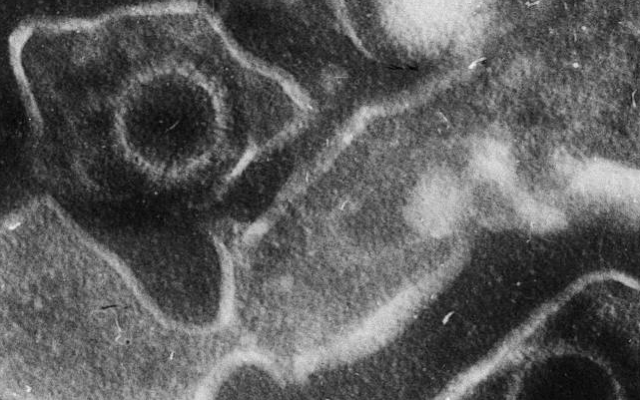
O vírus Epstein-Barr, também conhecido como herpesvírus humano 4, é o causador da mononucleose infecciosa, mas também está associado a alguns tipos de câncer, como o linfoma de Hodgkin.
O EBV pode, segundo os pesquisadores de Harvard, após a mononucleose infecciosa, "estabelecer uma infecção latente e vitalícia no hospedeiro".
O grande desafio do estudo foi estabelecer uma relação causal entre o vírus e a esclerose múltipla.
Isso porque se estima que o EBV infecte cerca de 95% dos adultos, enquanto a esclerose múltipla é uma doença relativamente rara, com sintomas que podem demorar até dez anos para surgir após o contato com o vírus.
Para determinar a conexão, os cientistas analisaram mais de 10 milhões de jovens adultos na ativa nas Forças Armadas dos EUA. Eles coletaram amostras de soro dos militares a cada dois anos.
Identificou-se que 955 deles foram diagnosticados com esclerose múltipla durante o período de serviço.
Como o acompanhamento foi periódico, eles conseguiram verificar desde o início quais já tinham tido contato com o EBV e os que tiveram contato ao longo do estudo.
Entre os que foram infectados pelo vírus Epstein-Barr no primeiro ano de serviço, o risco de esclerose múltipla aumentou em 32 vezes.
"Os achados não podem ser explicados por nenhum fator de risco conhecido para EM [esclerose múltipla] e sugerem o EBV como a principal causa de EM", acrescenta o comunicado.
A pesquisa abre caminho para uma abordagem preventiva em relação ao vírus Epstein-Barr, salienta o professor Ascherio.
“Atualmente, não há como prevenir nem tratar efetivamente a infecção pelo EBV, mas uma vacina contra o EBV ou direcionar o vírus com medicamentos antivirais específicos para o EBV poderia prevenir ou curar a EM.”
R7
Foto: Reprodução/PLoS

















