A harmonização facial está na moda entre os brasileiros e vem fazendo sucesso nos consultórios. O procedimento estético é um conjunto de tratamentos no rosto criado para melhorar a harmonia entre os dentes, boca e rosto de uma forma geral.
 O tratamento é feito de fora para dentro do rosto. “Primeiro é feita a aplicação nas bochechas, depois na região das têmporas até chegar ao bigode chinês”, explica a dermatologista e consultora do Bem Estar Márcia Purceli.
O tratamento é feito de fora para dentro do rosto. “Primeiro é feita a aplicação nas bochechas, depois na região das têmporas até chegar ao bigode chinês”, explica a dermatologista e consultora do Bem Estar Márcia Purceli.
Para o procedimento, as técnicas mais usadas são o ácido hialurônico, toxina botulínica, laser e peeling.
Não existe uma idade mínima para fazer a harmonização. Entretanto, pessoas mais velhas costumam procurar pelo procedimento por causa da flacidez e envelhecimento.
Decidi fazer a harmonização. Quais os riscos?
A dermatologista explica que o profissional escolhido para fazer a harmonização precisa ter conhecimento da anatomia da face. “A região tem muitos nervos e artérias. A aplicação errada pode provocar severas complicações. Se pegar um vaso sanguíneo, por exemplo, pode dar necrose e até cegueira”.
Fique atento:
Não faça procedimento quando estiver gripado, com sinusite, coriza ou fazendo tratamento dentário (são situações que abrem a porta para um microrganismo entrar)
Colocar muitas ampolas no mesmo dia pode ser perigoso
Não é normal: dor forte, inchaço e vermelhidão
Os hematomas podem ficar na pele de cinco a seis dias
Lembrando que a harmonização é contraindicada para grávidas, pessoas com doenças autoimunes e pessoas que tomam imunossupressores.
Bem Estar
Foto: Arte/TV Globo














 Cientistas da Universidade do Arkansas, nos Estados Unidos, desenvolveram um protótipo de laser capaz de destruir células cancerígenas que circulam na corrente sanguínea. A técnica é totalmente não-invasiva, ou seja, o procedimento é feito do lado de fora do corpo do paciente.
Cientistas da Universidade do Arkansas, nos Estados Unidos, desenvolveram um protótipo de laser capaz de destruir células cancerígenas que circulam na corrente sanguínea. A técnica é totalmente não-invasiva, ou seja, o procedimento é feito do lado de fora do corpo do paciente. A campanha nacional de vacinação contra a gripe terminou no fim de maio. Entretanto, a imunização ficou abaixo da meta. Com isso, as doses remanescentes foram disponibilizadas para toda a população.
A campanha nacional de vacinação contra a gripe terminou no fim de maio. Entretanto, a imunização ficou abaixo da meta. Com isso, as doses remanescentes foram disponibilizadas para toda a população.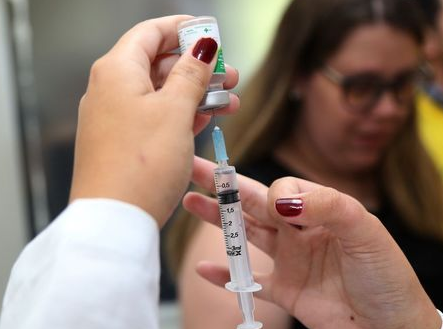 O vírus H1N1 causou 67% das mortes por gripe este ano no país. Até o último informe epidemiológico do Minitério da Saúde, de 25 de maio, 222 pessoas morreram em decorrência da gripe, sendo 148 pelo vírus.
O vírus H1N1 causou 67% das mortes por gripe este ano no país. Até o último informe epidemiológico do Minitério da Saúde, de 25 de maio, 222 pessoas morreram em decorrência da gripe, sendo 148 pelo vírus.