A Agência Nacional de Vigilância Sanitária (Anvisa) informou hoje (19) que aprovou, na última sexta-feira (16), um novo ensaio clínico de vacina contra a covid-19.

A vacina candidata terá duas doses com intervalo de 22 dias entre elas. O desenvolvimento clínico está sendo patrocinado pela empresa Sichuan Clover Biopharmaceuticals, sediada na China.
O ensaio clínico aprovado é controlado por placebo, para avaliar a eficácia, imunogenicidade e segurança da vacina, em participantes a partir de 18 anos de idade.
Nesta fase, devem ser incluídos até 22 mil voluntários distribuídos entre países da América Latina, além da África do Sul, Bélgica, China, Espanha, Polônia e Reino Unido.
No Brasil, serão 12,1 mil voluntários, distribuídos nos estados do Rio Grande do Sul, Rio Grande do Norte e Rio de Janeiro.
Análise
Para a aprovação do ensaio clínico, a Anvisa informou que realizou reuniões com a equipe da farmacêutica, a fim de alinhar todos os requisitos técnicos necessários para os testes.
Segundo a Anvisa, desde o reconhecimento de calamidade pública no Brasil em virtude da pandemia do novo coronavírus, a agência tem adotado estratégias para dar celeridade às análises e às decisões sobre qualquer demanda que tenha como objetivo o enfrentamento da covid-19.
“Uma dessas estratégias foi a criação de um comitê de avaliação de estudos clínicos, registros e mudanças pós-registros de medicamentos para prevenção ou tratamento da doença. O grupo também atua em ações para reduzir o risco de desabastecimento de medicamentos com impacto para a saúde pública devido à pandemia”, acrescentou.
Autorização
Para esta autorização, a Anvisa analisou os dados das etapas anteriores de desenvolvimento do produto, incluindo estudos in vitro e em animais, bem como dados preliminares de estudos clínicos em andamento. Os resultados obtidos até o momento demonstraram um perfil de segurança aceitável das vacinas candidatas.
Este é o sexto estudo de vacina contra o novo coronavírus autorizado pela Anvisa. As últimas autorizações foram: no dia 2 de junho de 2020, para o ensaio clínico da vacina desenvolvida pela Universidade de Oxford e a empresa Astrazeneca; em 3 de julho, para a vacina da Sinovac Research & Development, em parceria com o Instituto Butantan; em 21 de julho para a vacina da Pfizer/Wyeth; em 18 de agosto para a vacina da Janssen-Cilag; e em 8 de abril para a vacina da Medicago R&D.
Agência Brasil














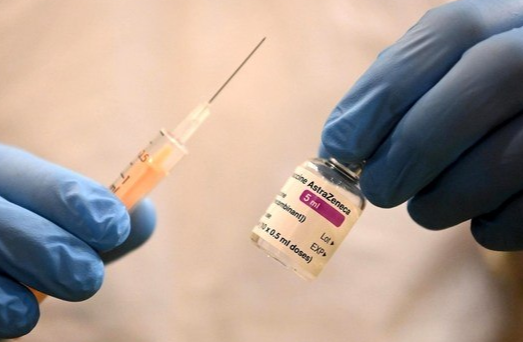 Uma versão modificada da vacina contra a covid-19 da AstraZeneca, desenvolvida para combater uma variante do coronavírus documentada pela primeira vez na África do Sul, pode estar pronta no final de 2021, disse uma funcionária da AstraZeneca na Áustria, em uma entrevista publicada neste domingo (18).
Uma versão modificada da vacina contra a covid-19 da AstraZeneca, desenvolvida para combater uma variante do coronavírus documentada pela primeira vez na África do Sul, pode estar pronta no final de 2021, disse uma funcionária da AstraZeneca na Áustria, em uma entrevista publicada neste domingo (18). O secretário de Atenção Primária à Saúde do Ministério da Saúde, Raphael Parente, pediu, nesta sexta-feira (16), que as mulheres adiem a gravidez até haver uma melhora da pandemia, se for possível.
O secretário de Atenção Primária à Saúde do Ministério da Saúde, Raphael Parente, pediu, nesta sexta-feira (16), que as mulheres adiem a gravidez até haver uma melhora da pandemia, se for possível.