 A Pfizer e a parceira alemã BioNTech disseram nesta segunda-feira (16) que apresentaram dados primários de um teste de estágio inicial à FDA (Agência de Alimentos e Medicamentos dos Estados Unidos), como parte de uma solicitação que pede autorização para uma dose de reforço de sua vacina contra a covid-19.
A Pfizer e a parceira alemã BioNTech disseram nesta segunda-feira (16) que apresentaram dados primários de um teste de estágio inicial à FDA (Agência de Alimentos e Medicamentos dos Estados Unidos), como parte de uma solicitação que pede autorização para uma dose de reforço de sua vacina contra a covid-19.
Os dados também serão submetidos à EMA (Agência Europeia de Medicamentos) e a outras autoridades regulatórias nas próximas semanas, disseram as farmacêuticas.
No teste, a terceira dose desencadeou anticorpos neutralizantes consideravelmente maiores contra o vírus SARS-CoV-2 original na comparação com os níveis observados após a série primária de duas doses, assim como contra as variantes Beta (África do Sul) e Delta (Índia), segundo os laboratórios.
Todos os pacientes receberam a terceira dose da vacina da Pfizer/BioNTech de oito a nove meses depois da administração da segunda dose.
Os resultados de um teste de estágio avançado de avaliação da terceira dose são esperados para breve e serão apresentados à FDA, EMA e outras autoridades regulatórias de todo o mundo, disseram as empresas.
Na semana passada, autoridades regulatórias dos EUA autorizaram uma terceira dose das vacinas contra covid-19 da Pfizer/BioNTech e da Moderna para pessoas com imunidade comprometida que provavelmente têm uma proteção menor dos regimes de duas doses.
Reuters
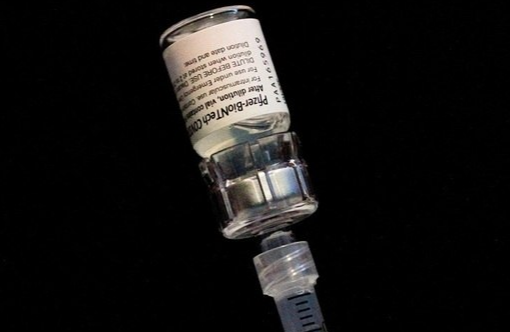
Foto: MARCO BELLO/REUTERS













